
Die Europäische Datenbank für Medizinprodukte (EUDAMED) spielt eine entscheidende Rolle bei der Regulierung und Überwachung von Medizinprodukten innerhalb der Europäischen Union. Mit der Einführung der Verordnungen (Art. 26 der MDR 2017/745 und Art. 23 der IVDR 2017/746) sind die EMDN-Codes (European Medical Device Nomenclature) innerhalb dieses Systems von großer Bedeutung geworden.
Was sind EMDN-Codes und warum sind sie wichtig?
Die EMDN-Codes sind ein unverzichtbarer Bestandteil der europäischen Normierung im Bereich der Medizinprodukte. Sie repräsentieren die European Medical Device Nomenclature – eine einheitliche Klassifizierung und Bezeichnung von Medizinprodukten. Die Grundlage für die EMDN bildet die italienische CND-Nomenklatur. Bei der Registrierung ihrer Medizinprodukte in EUDAMED müssen Hersteller diese Codes zwingend angeben. Jede UDI-DI (Unique Device Identification – Device Identifier) muss mit einem entsprechenden EMDN-Code verknüpft werden.
Die Implementierung der EMDN-Codes hat das Ziel, die Suchvorgänge für Benutzer zu erleichtern, die die GMDN (Global Medical Device Nomenclature) verwenden. Dafür wird eine Zuordnung (Mapping) zwischen den EMDN- und GMDN-Codes hergestellt, um eine klare Übersicht für alle Akteure zu ermöglichen. In der Praxis ermöglichen diese Codes eine standardisierte und eindeutige Identifikation von Produkten, was wiederum die Kommunikation, Verfolgung und Überwachung von Medizinprodukten auf dem gesamten europäischen Markt erheblich erleichtert.
Finden Sie hier die vollständige Nomenklatur.
Wie funktionieren EMDN-Codes, wie werden sind diese aufgebaut?
Die EMDN-Codes werden auf Grundlage spezifischer Kriterien generiert, die Produktmerkmale, Verwendungszwecke und weitere relevante Informationen berücksichtigen. Diese Codes bestehen aus einer alphanumerischen Kombination und folgen einem hierarchischen System. Die Länge der EMDN-Codes beträgt zwischen 3 und 14 Zeichen, wobei das erste Zeichen ein Großbuchstabe sein muss und die folgenden Zeichen numerisch sind.
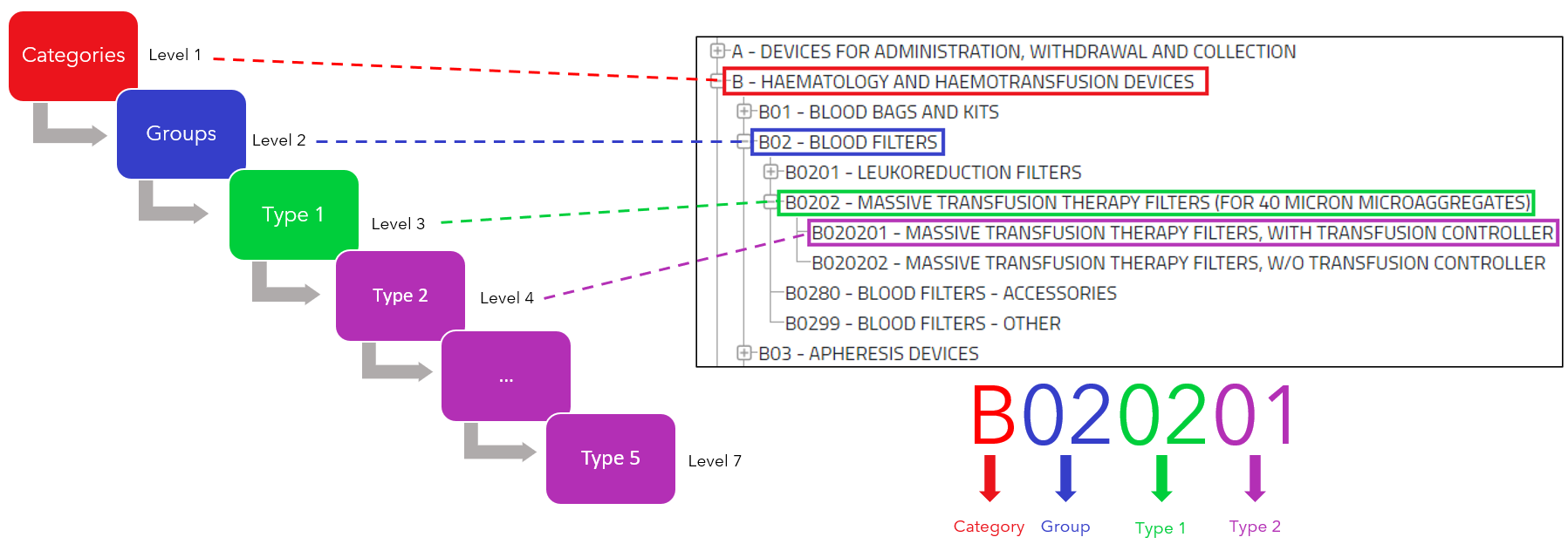
Die Struktur der EMDN-Codes folgt einem abgestuften Muster, das von allgemeinen zu spezifischen Informationen führt. Hierbei ist es wichtig zu beachten :
- dass „Kategorie“ nicht mit „Kategorie des Geräts“ gleichzusetzen ist
- und „Gruppe“ nicht mit „generischen Gerätegruppen“ verwechselt werden sollte.
Diese baumartige Hierarchie spielt eine zentrale Rolle bei der Zuordnung eines passenden Begriffs bzw. Codes zu einem Gerät. Hersteller sind daher gefordert, möglichst präzise und detaillierte Begriffe bzw. Codes zu verwenden.
Wir haben ein Video vorbereitet, das Ihnen genau zeigt, wie Sie die EMDN-Codes in unserem SAP EUDAMED Add-On hinzufügen
Wir haben ebenfalls ein 2 Video vorbereitet, das Ihnen genau zeigt, wie Sie die EMDN-Codes in dem EUDAMED Playground hinzufügen
Die Einführung der EMDN-Codes in EUDAMED markiert einen bedeutsamen Schritt in der Regulierung von Medizinprodukten innerhalb der EU.
Finden Sie auch hier die aktuelle MDCG-FAQ zum EMDN.





Related Posts