
La identificación y trazabilidad de los dispositivos médicos son factores cruciales para la seguridad y eficiencia del paciente en la cadena de suministro de la industria de dispositivos médicos. En este contexto, los códigos de barras de identificación única de dispositivos desempeñan un papel central.
¿Por qué son necesarios los códigos de barras UDI y el etiquetado UDI correcto?
La introducción de los códigos de barras UDI y el etiquetado correspondiente es parte de los requisitos UDI y la regulación MDR que los fabricantes de dispositivos médicos deben cumplir. Estos requisitos regulatorios son especialmente aplicados por la FDA, EUDAMED y otras regulaciones globales.
En particular, el reglamento MDR 2017/745 de la UE proporciona especificaciones precisas y detalladas para los códigos de barras/etiquetas UDI correctos. Comprender esto es crucial para seguir cumpliendo con el MDR de la UE.
¿Qué tipos de códigos de barras existen?
¿Qué tipos de códigos de barras están disponibles para UDI?
La elección del tipo de código de barras es crucial, ya que los diferentes códigos de barras admiten diferentes cantidades de información y escenarios de aplicación. Estos son los diferentes tipos de códigos de barras que desempeñan un papel en la implementación de los requisitos de UDI:
- Matriz de datos (estándar de la industria): la matriz de datos es uno de los tipos de códigos de barras clave en la industria de dispositivos médicos y se considera un estándar de la industria. Este código de barras bidimensional, que puede ser cuadrado o rectangular, es conocido por su alta capacidad de almacenamiento de datos y robustez. Data Matrix permite el almacenamiento de información extensa en un espacio pequeño, incluido el código UDI, los números de lote, los números de serie, las fechas de caducidad y las fechas de fabricación, lo que es especialmente ventajoso para dispositivos médicos pequeños.

- Código QR: El Código de Respuesta Rápida (Código QR) es otro tipo de código de barras ampliamente utilizado conocido por su rápida legibilidad y gran capacidad de información. Los códigos QR se utilizan comúnmente con fines de marketing, pero también encuentran aplicación en la industria de dispositivos médicos. Proporcionan la capacidad de codificar información adicional como el origen, el número de lote o la fecha de vencimiento. El código QR se utiliza a menudo en el sistema UDI chino.
- Código 128: El código 128 es un código de barras lineal que permite una alta densidad de datos. Este tipo de código de barras se utiliza a menudo en situaciones en las que se necesita codificar una gran cantidad de datos alfanuméricos. Code 128 es flexible y admite varios conjuntos de caracteres, lo que lo hace adecuado para la identificación, el etiquetado y la transmisión de información sobre productos sanguíneos, tejidos humanos y órganos.

Diferentes entidades emisoras:
En la implementación de los requisitos de UDI, los organismos emisores también desempeñan un papel crucial. Las agencias emisoras conocidas incluyen GS1 y HIBCC. La elección del Organismo Emisor influye directamente en el tipo de código de barras utilizado:
- GS1: GS1 es una organización que opera a nivel mundial y que establece estándares para la identificación de productos. Cuando se utilizan códigos GS1, se deben utilizar tipos de códigos de barras GS1 como GS1 Data Matrix, GS1 QR Code y GS1 Code 128. Esto garantiza el cumplimiento de las normas GS1 y la identificación coherente del producto.
- HIBCC: El Consejo de Comunicaciones Empresariales de la Industria de la Salud (HIBCC) es una agencia emisora especializada en el sector de la salud. Dependiendo de los requisitos y acuerdos específicos, puede ser necesario el uso de códigos HIBCC y los tipos de códigos de barras correspondientes.

¿Qué datos deben imprimirse en una etiqueta UDI?
El diseño y el contenido de una etiqueta UDI son cruciales para la identificación y trazabilidad únicas de los dispositivos médicos. Ciertos datos deben presentarse de manera precisa y legible en una etiqueta UDI.
1. Símbolos
Un elemento central en una etiqueta UDI es el uso de varios símbolos. Estos símbolos representan información como fabricante, representante de la UE, importador, distribuidor, etc. La representación clara de estos símbolos garantiza una captura de datos rápida y precisa por parte de los escáneres y otros dispositivos de lectura.


2. Información textual:
Además de los símbolos, la información textual también debe estar presente en la etiqueta. Esto puede incluir información del producto, como el nombre del producto, el fabricante, la fecha de caducidad y otros detalles relevantes. Esta información debe presentarse en una fuente clara y legible.
Ejemplo: El origen de un producto médico se puede etiquetar de la siguiente manera:
Hecho en CC (donde CC es el código de país de ISO 3166-1)
3. HRI (Interpretación legible por humanos):
HRI significa Interpretación legible por humanos e interpreta el UDI como símbolos que pueden ser leídos por los humanos. Es la representación textual del contenido del código de barras. Esto significa que los datos contenidos en el código de barras se reproducen en forma legible por humanos en la etiqueta. Esto es particularmente importante para los usuarios que necesitan verificar manualmente la información, por ejemplo, durante el almacenamiento, en la atención médica o cuando usan dispositivos médicos.

Ventajas de usar símbolos en lugar de texto:
El uso de símbolos en lugar de texto ofrece varias ventajas, especialmente en un contexto internacional. Un ejemplo es el símbolo de "Un solo uso". En lugar de enumerar el texto "Uso único" en diferentes idiomas, se puede usar un símbolo uniforme . Esto no solo optimiza el espacio disponible en la etiqueta, sino que también reduce significativamente el esfuerzo para las etiquetas multilingües. El uso constante de símbolos reconocidos internacionalmente también promueve la comprensión universal.
Nuevo símbolo según ISO 15223-1:
La ISO 15223-1 es la más importante de las normas mencionadas y actualmente se encuentra en proceso de coordinación para la versión 2020. Además de los cambios en las definiciones de símbolos existentes, se añadirán algunos símbolos nuevos. Los símbolos específicos que se añadirán solo se conocerán después de la publicación. Hemos enumerado algunos de los símbolos que se espera que se incluyan en la nueva norma en la siguiente tabla.

¿Qué son UDI-DI y UDI-PI? ¿Qué los distingue?
El UDI permite la identificación y trazabilidad únicas en todo el mundo de dispositivos médicos. El UDI debe imprimirse como un código de barras y en texto sin formato. Se permiten todos los formatos de código de barras siempre y cuando la estructura de datos siga la norma ISO 15418.
El número UDI incluye dos componentes:
- UDI-DI: Identificador de dispositivo, Identificador de producto estático (por ejemplo, GTIN)
El identificador de dispositivo (ID) es un código único asignado a un dispositivo médico específico. Este código permite la identificación y diferenciación única de un producto específico de otros productos del mismo tipo. Garantiza que se pueda realizar un seguimiento individual de cada producto.
- UDI-PI: Identificador Dinámico de Producto (por ejemplo, Lote No., n .º de serie, fecha de producción, etc.)
El identificador de producción (IP) complementa el identificador del dispositivo e incluye información sobre el proceso de fabricación y los lotes del dispositivo médico. El PI varía según los requisitos del fabricante y puede incluir datos como números de lote, números de serie, fechas de fabricación y fechas de vencimiento.

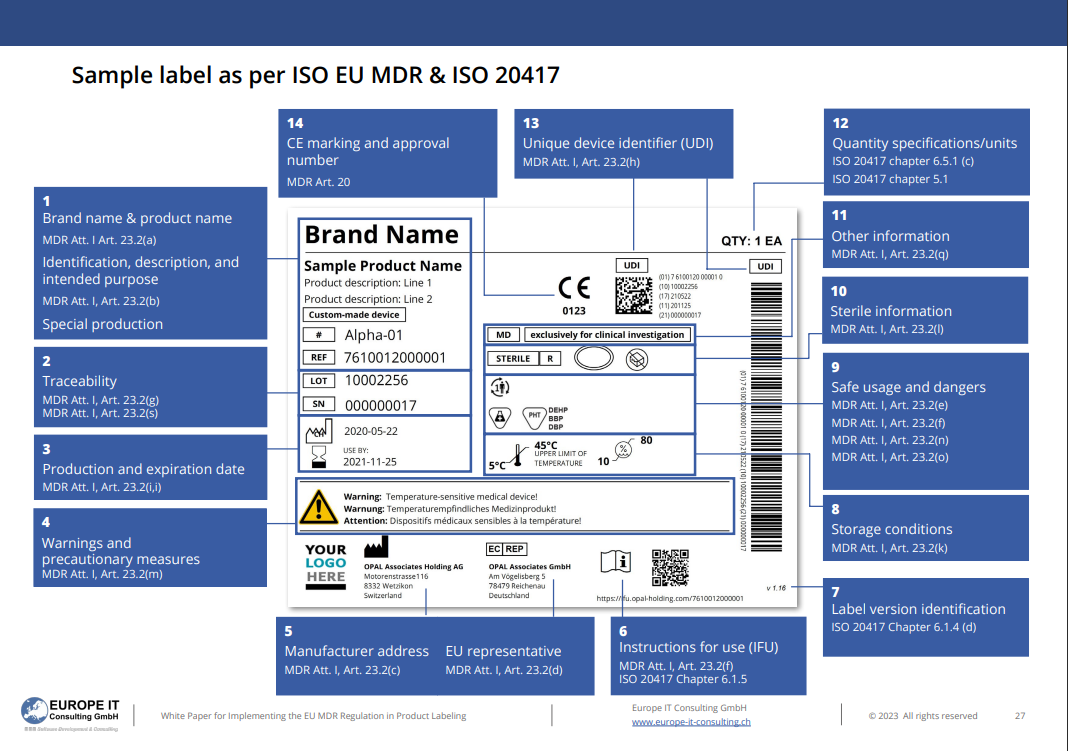
Muestra de la etiqueta UDI
Europe IT ha preparado una muestra para usted para que pueda tener una idea concreta de cómo debe verse la etiqueta de acuerdo con ISO EU MDR e ISO 20417.
¡Responde a nuestro cuestionario interactivo en solo 5 minutos!
Ponga a prueba sus conocimientos con 15 preguntas rápidas y descubra dónde se encuentran sus conocimientos sobre el tema del código de barras y las etiquetas UDI. Nuestro cuestionario cubre varios aspectos, desde los principios básicos hasta las regulaciones aplicables. Es una gran oportunidad para que los profesionales de la industria, las autoridades reguladoras y los curiosos obtengan más información.
Guía para implementar la regulación MDR de la UE en el etiquetado de productos
Las etiquetas UDI y los códigos de barras desempeñan un papel crucial en el cumplimiento de los requisitos de UDI. Europe IT Consulting ha publicado recientemente un Libro Blanco "Guía para implementar la regulación MDR de la UE en el etiquetado de productos", que proporciona información detallada e información completa. Regístrese ahora para acceder a este documento técnico:
