Die Umsetzung der Medizinprodukteverordnung geht mit einer neuen EMDN (European Medical Device Nomenclature) einher, als in den Verordnungen (Art.26 2017/745 MDR, Art.23 2017/746 IVDR) festgelegt. Erfahren Sie dieses Konzept hier, und erfahren Sie, was diese Änderung für Sie als EUDAMED-Akteur bedeutet.
Die Implementierung der EMDN erfolgt, um die Codesuche durch Bediener zu erleichtern, die die GMDN (Global Medical Device Nomenclature; der internationale Standard zur Benennung von Medizinprodukten) verwenden. Daher wird die EMDN auf die GMDN gemappt, so dass die Entsprechung zwischen diesen beiden für alle Bediener sichtbar sein kann. Die Basis bleibt jedoch die italienische CND-Nomenklatur, die 2019 von der MDCG als solche für das EMDN ausgewählt wurde.
Sobald EUDAMED vollständig online geht, muss diese neue Nomenklatur von den Herstellern verwendet werden, wenn sie Medizinprodukte in der EUDAMED-Datenbank registrieren. Jede UDI-DI muss mit einem Code verknüpft werden.
Finden Sie hier die vollständige Nomenklatur.
Vorteile:
Auch wenn die Nomenklatur umständlich erscheinen mag, ist sie letztlich für alle von Vorteil. Für die Hersteller spielt die EMDN eine wesentliche Rolle in der technischen Dokumentation, da sie für Struktur und Organisation sorgt. Auf der anderen Seite unterstützt sie in hohem Maße die Patienten, indem sie wichtige Beschreibungen zu allen in EUDAMED registrierten Geräten liefert.
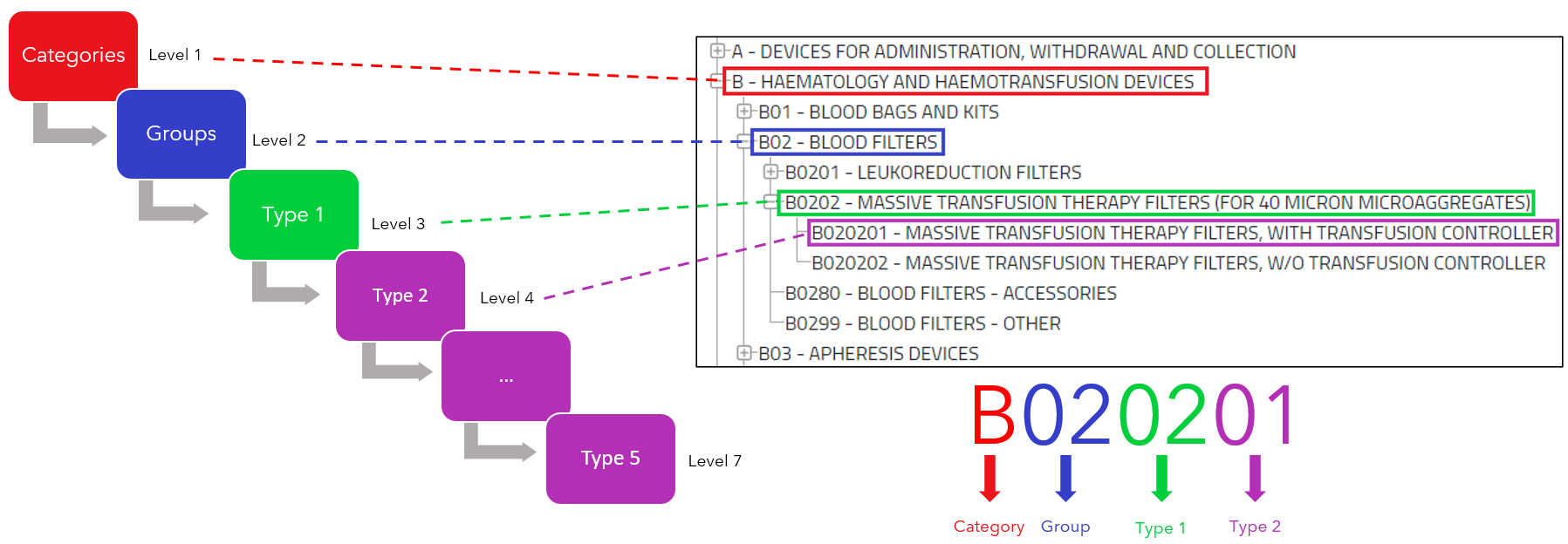
Aufbau der Codes:
Hier ein Beispiel, wie die EMDN-Codes aufgebaut sind:
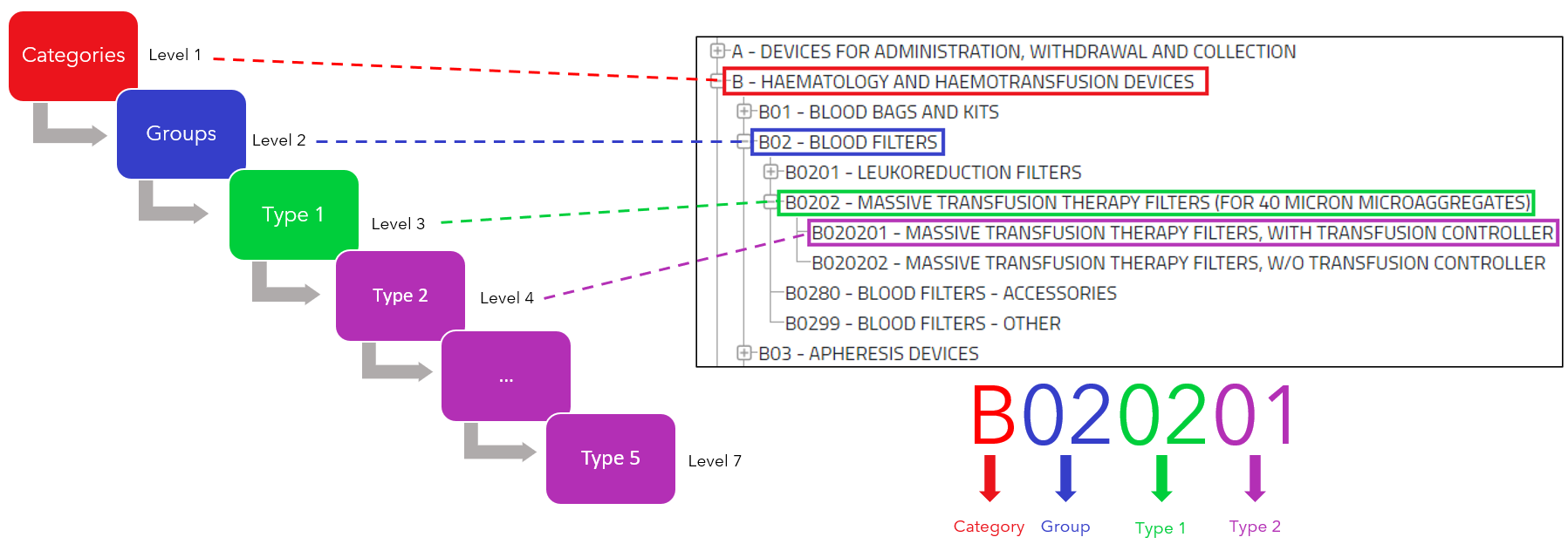
Der Aufbau des Codes geht vom Allgemeinen zum Speziellen.
Beachten Sie das:
- „Kategorie“ ≠ „Kategorie des Geräts“.
- „Gruppe“≠ „generische Gerätegruppen“.
Diese baumartige Hierarchie muss berücksichtigt werden, wenn es darum geht, einem Gerät einen Begriff zuzuordnen. Das heißt, der Hersteller muss einen möglichst detaillierten und präzisen Begriff bzw. Code vergeben.
Die Europäische Kommission führt derzeit eine Konsultation über die Qualität dieser neuen Nomenklatur durch. Die zweite Version der EMDN wird dann im 3. Quartal 2021 veröffentlicht werden. Gleichzeitig werden die Kategorien J,W und Z um neue Begriffe zur Beschreibung von Medizinproduktesoftware ergänzt.
Finden Sie auch hier die aktuelle MDCG-FAQ zum EMDN.








Related Posts